L’oxygénothérapie hyperbare est une thérapie puissante dont les bénéfices pour notre santé peuvent être nombreux. Les avancées scientifiques sur le sujet s’enchainent et démontrent qu’il serait même possible de déclencher des mécanismes de réparation au niveau cellulaire. Ce qui est très intéressant pour notre corps et notre cerveau ! Dans cet article nous allons découvrir plus en détails les effets du caisson hyperbare sur nos cellules et ce qui dit la science à ce sujet.
Nos cellules ont besoin d’oxygène
Saviez-vous que l’oxygène est le troisième élément le plus abondant dans l’univers, après l’hydrogène et l’hélium ? Il y a environ 300 millions d’années, le taux d’oxygène dans l’air était de 35%, ce qui pourrait avoir contribué à la grande taille des animaux et des insectes de l’époque1https://www.ncbi.nlm.nih.gov/pmc/articles/PMC34224/. Aujourd’hui, l’oxygène constitue 20,8% de l’atmosphère terrestre.

Crédit photo : Jcomp – Freepik.com
Au cours de l’évolution, tous les mammifères se sont adaptés afin de pouvoir fournir un niveau d’oxygène optimal aux cellules de leur organisme. Chez l’humain, la chaîne de distribution d’oxygène commence au niveau des poumons, et finit dans les mitochondries de nos cellules.
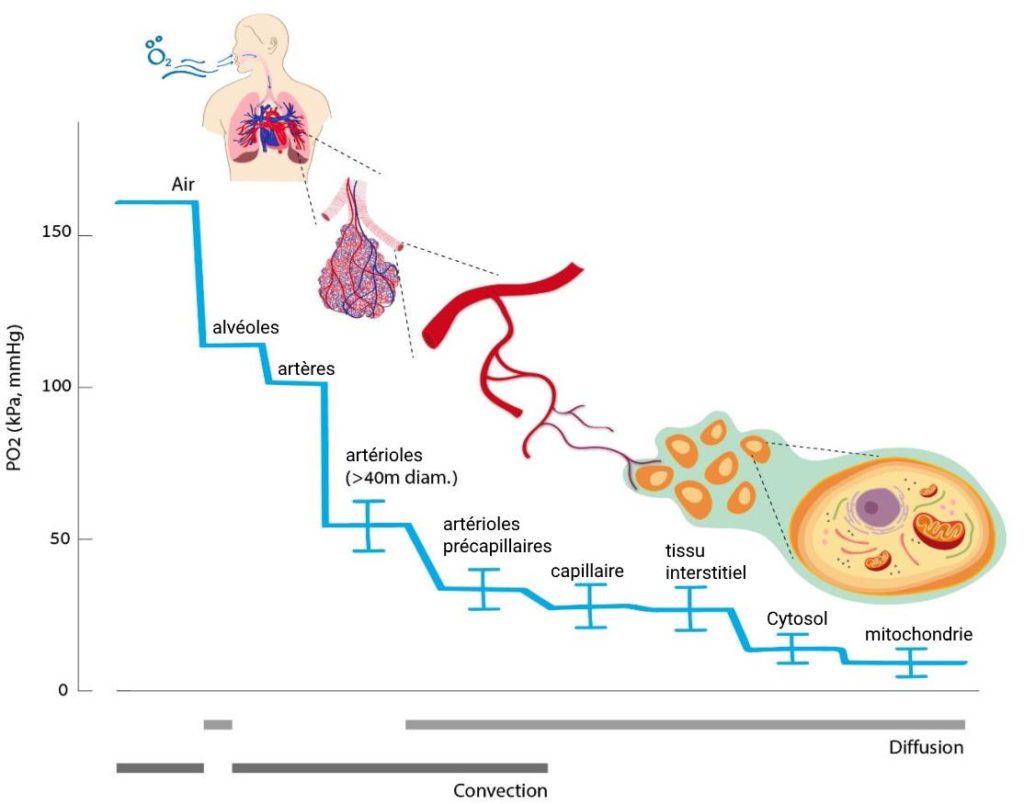
Crédit : Biomolecules. 2020 Jun, doi: 10.3390/biom10060958
Ces petites centrales énergétiques utilisent 80% de l’oxygène que l’on respire, ainsi que les aliments que nous ingérons, afin de produire de l’énergie (ATP). C’est ce qu’on appelle la respiration cellulaire.
La demande cellulaire en oxygène peut varier en fonction des besoins. Par exemple, un muscle en exercice a une demande en oxygène plus élevée qu’un muscle au repos. Par conséquent, il existe plusieurs mécanismes et réflexes permettant au corps humain de maintenir un apport adéquat en oxygène. Parmi eux, l’augmentation de la ventilation et la dilatation des artères pulmonaires2https://pubmed.ncbi.nlm.nih.gov/18036551/.
Notre capacité à maintenir un apport constant en oxygène est essentielle au bon fonctionnement de nos cellules… et à notre survie ! Mais que se passe t-il lorsque nos cellules manquent d’oxygène ?
La réponse cellulaire face à l’hypoxie
L’importance fondamentale de l’oxygène est connue depuis des siècles, mais la découverte de la façon dont le corps s’adapte à sa disponibilité ne date que de 19383https://www.nobelprize.org/prizes/medicine/1938/heymans/facts/. Pire, la réaction cellulaire au manque d’oxygène, appelée hypoxie, n’a été éclaircie que récemment. En effet, ce n’est qu’en 2019 qu’une équipe de 3 scientifiques a été récompensée par le prix Nobel de physiologie ou médecine4https://www.nobelprize.org/prizes/medicine/2019/summary/ pour l’ensemble de leurs travaux sur le sujet. Après presque 3 décennies de recherche, ils ont pu enfin comprendre les mécanismes déclenchés au niveau cellulaire !
Facteur induit par l’hypoxie (HIF)
Avertissement : avant de continuer la lecture de cet article, gardez à l’esprit que le but est de vulgariser et de rendre l’information accessible à tous. Si vous avez des connaissances poussées en biologie, je vous invite à consulter directement les sources scientifiques disponibles à la fin de l’article.
En fonction de la disponibilité de l’oxygène, un complexe de protéines nommé HIF-1α, se retrouve en plus ou moins grande quantité à l’intérieur de nos cellules :
- À des niveaux d’oxygène normaux, les protéines HIF-1α sont dégradées par un processus cellulaire appelée protéasome.
- Lorsque les niveaux d’oxygène sont faibles, notre corps dispose de moins de dérivés réactifs de l’oxygène (ROS en anglais) afin de dégrader ce complexe HIF-1α. De ce fait, sa quantité augmente et le signal d’alarme est sonné ! HIF-1α fini par activer certains gènes codés dans notre ADN.
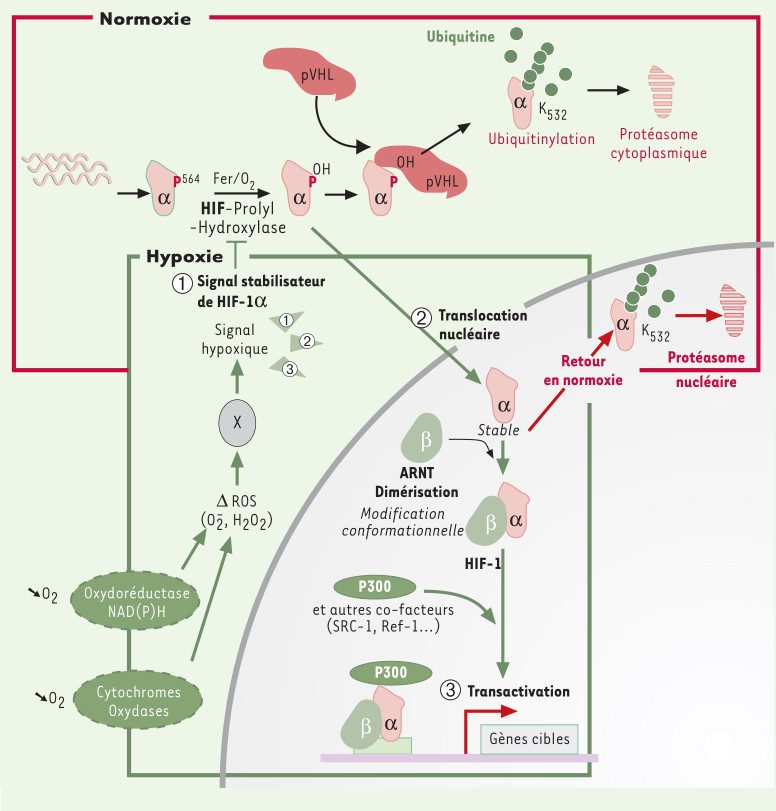
Les protéines qui activent des gènes sont appelées des facteurs de transcription5https://fr.wikipedia.org/wiki/Facteur_de_transcription. Et justement, en cas d’hypoxie prolongée (par exemple des alpinistes passant plusieurs jours en montagne), le facteur induit par l’hypoxie (HIF en anglais)6https://en.wikipedia.org/wiki/Hypoxia-inducible_factor active plus d’une centaine de gènes qui sont essentiels à notre survie 7https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6586788/.
Le HIF est le véritable chef d’orchestre de la réaction cellulaire à l’hypoxie
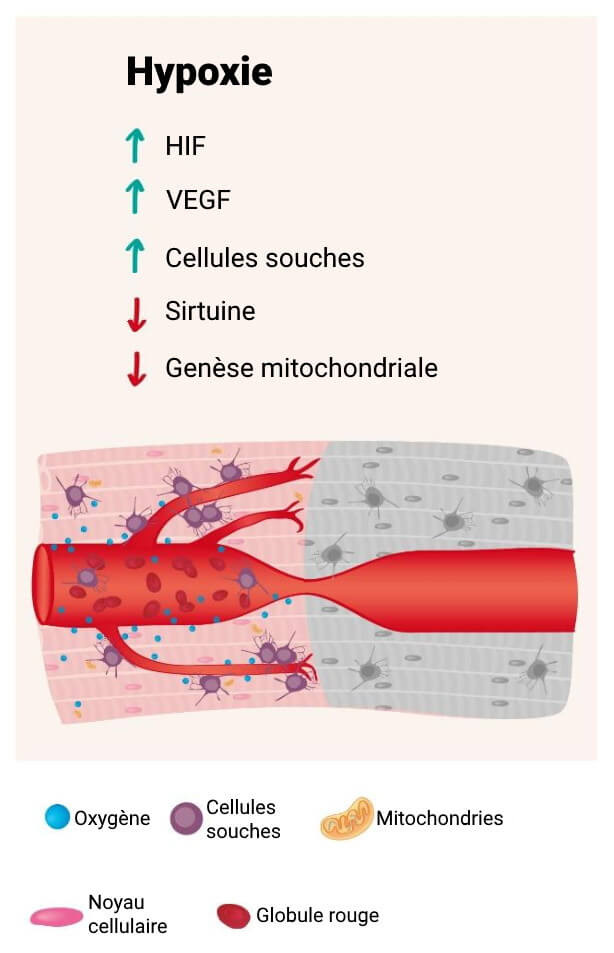
En plus de stimuler de nombreux gènes, le facteur induit par l’hypoxie déclenche d’important processus de régénération dans notre corps :
- Le facteur de croissance endothélial vasculaire (VEGF), qui permet la formation de nouveaux vaisseaux depuis un réseau préexistant. On appelle cela l’angiogenèse8https://pubmed.ncbi.nlm.nih.gov/18504100/.
- La prolifération et la migration de cellules souches9https://pubmed.ncbi.nlm.nih.gov/19698058/.
Néanmoins, l’hypoxie prolongée apporte aussi son lot d’effets négatifs au niveau cellulaire :
- Une diminution de la biogenèse mitochondriale et du nombre de mitochondries10https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6453877/.
- Nos sirtuines sont aussi régulées à la baisse. Les sirtuines sont des enzymes qui régulent un large éventail de processus biologiques, allant de la transcription des gènes au métabolisme énergétique11https://www.frontiersin.org/articles/10.3389/fphys.2021.752117/full.
Ainsi, comme vous pouvez le constater, l’hypoxie est le déclencheur naturel d’importants processus métaboliques. Positifs (déclenchés grâce au HIF), mais aussi négatifs (déclenchés par le manque d’O2 !).
Le paradoxe hypoxique hyperoxique
Et maintenant, si je vous disais qu’il est possible de tromper nos cellules ? À l’aide d’un caisson hyperbare, il est possible d’activer ce fameux HIF, mais sans être en état d’hypoxie…
Nous avons vu un peu plus haut que nos cellules ont la faculté de détecter l’hypoxie prolongée. Et fort heureusement pour nous, cette faculté est faillible ! En effet, les cellules interpréteraient de la même façon les 2 situations suivantes :
- Passer d’un état où l’oxygène est disponible, à un état où il en manque.
- Passer d’un état où notre corps est sur-oxygéné en caisson hyperbare (hyperoxie), à un état normal (normoxie).
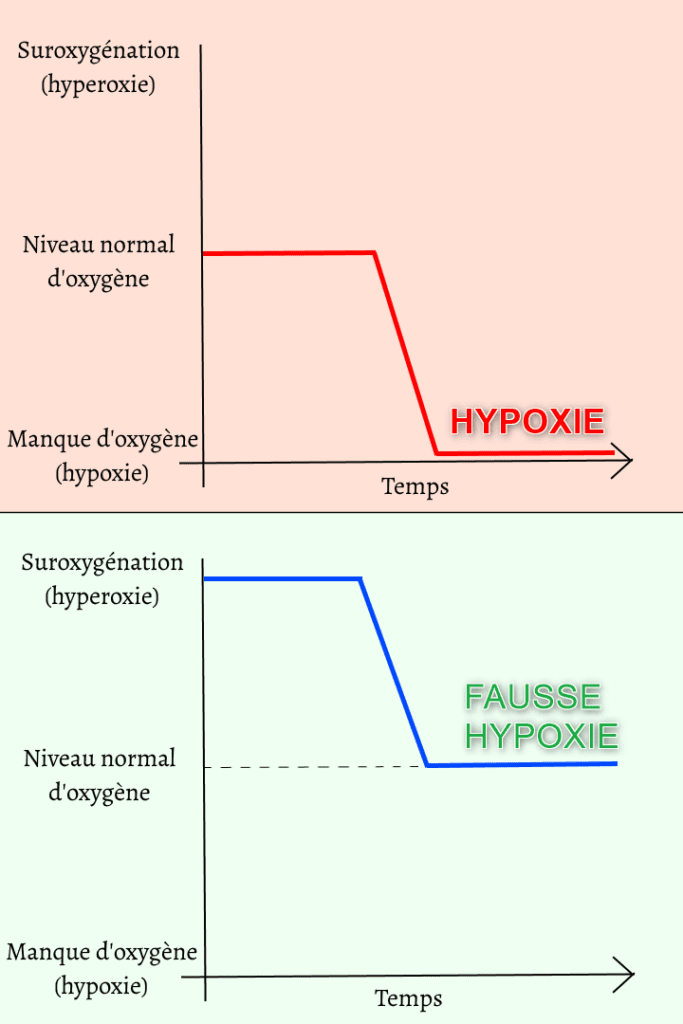
Ainsi, passer de l’hyperoxie à la normoxie permettrait d’activer le HIF et de déclencher la cascade de processus de régénération. Tout en évitant l’hypoxie !
C’est ce qu’on appelle le paradoxe hypoxique hyperoxique12https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7355982.
Les effets du paradoxe hypoxique hyperoxique sur nos cellules
Les chercheurs expliquent les effets du paradoxe hypoxique hyperoxique sur nos cellules à l’aide de l’hypothèse suivante :
- Dans des conditions normoxiques, l’oxygène et les dérivés réactifs de l’oxygène sont disponibles. La dégradation de HIF-1α a donc bien lieu.
- Pendant l’hyperoxie en caisson hyperbare, la disponibilité en oxygène est accrue, ce qui améliore naturellement notre production de dérivés réactifs de l’oxygène et d’antioxydants.
- De retour à la normoxie après une seule exposition hyperoxique, le rapport entre les dérivés réactifs de l’oxygène et les antioxydants sera élevé.
- Lors du retour à la normoxie suite à des expositions hyperoxiques répétées, le rapport entre les dérivés réactifs de l’oxygène et les antioxydants sera faible. Ce qui est similaire à un état hypoxique ! La dégradation des protéines HIF-α n’a donc pas lieu et le signal d’alarme (HIF) est alors déclenché !

Cela signifie que l’hyperoxie intermittente et répétée en caisson hyperbare simule l’hypoxie en déséquilibrant le rapport entre les dérivés réactifs de l’oxygène et les antioxydants.
Quels sont les effets du caisson hyperbare sur nos cellules ?
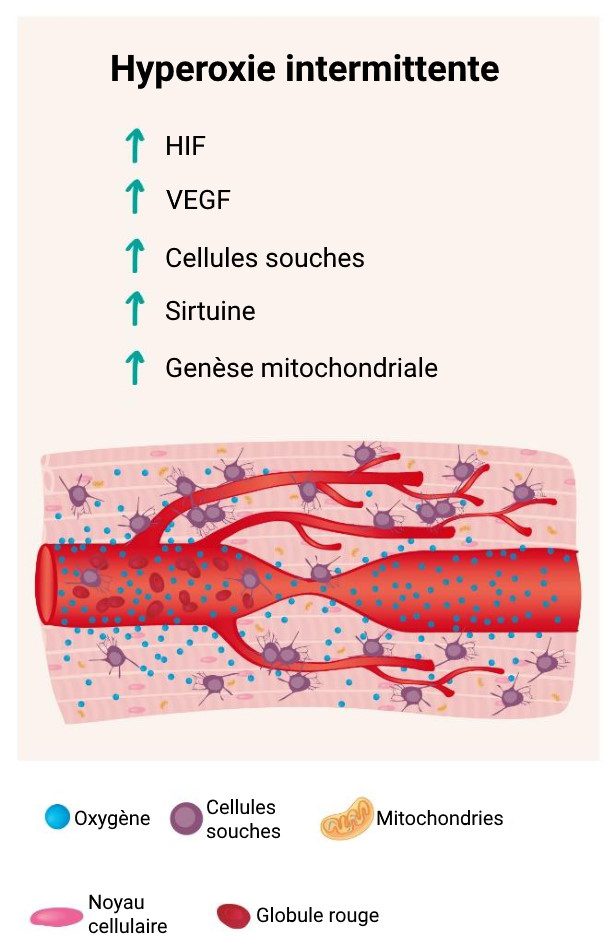
Les effets bénéfiques du paradoxe hypoxique hyperoxique sont multiples. Voici quelques exemples tirés de la littérature scientifique :
- HIF : l’effet de l’hyperoxie intermittente répétée en caisson hyperbare a été démontré sur différents types d’organes et de cellules. Par exemple, sur les cellules de cerveaux abîmés13https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4102647, de l’appareil digestif14https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5021505/ et du foie15https://pubmed.ncbi.nlm.nih.gov/18644387/.
- VEGF : L’angiogenèse est stimulée après des expositions hyperoxiques intermittentes. L’oxygénothérapie hyperbare peut initier les mécanismes de réparation cellulaire et vasculaire pour induire l’angiogenèse cérébrale et améliorer le flux sanguin dans les régions cérébrales endommagées16https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5654341/.
- Cellules souches : L’hypoxie et l’hyperoxie intermittentes stimulent la prolifération de cellules souches. Des études sur des patients souffrant de lésions cérébrales ont démontré que des séances répétées en caisson hyperbare augmentaient le nombre de cellules souches circulantes, et qu’il y avait une corrélation avec les améliorations cliniques observées17https://pubmed.ncbi.nlm.nih.gov/28779582/.
- Sirtuine : Des expositions hyperoxiques intermittentes stimulent l’activité des sirtuines. Ces dernières ont un effet neuroprotecteur qui a été étudié sur plusieurs modèles animaux. Les sirtuines entraînent une atténuation de l’infarctus cérébral et améliorent la fonction neurologique18https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5489129/.
- Mitochondries : l’oxygénothérapie hyperbare permet de délivrer beaucoup plus d’oxygène aux mitochondries. De ce fait, cette thérapie induit la biogenèse et la migration des mitochondries, ce qui participe au maintien de la fonction neuronale19https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4084443 20https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4968589 21https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6630002.
Vous savez maintenant pourquoi les séances en caisson hyperbare sont régénératrices !
Conclusion
De nombreuses avancées ont été faites ces dernières années concernant l’oxygénothérapie hyperbare. Observer les progrès et les améliorations qui profitent aux patients est une chose importante. Mais nous devons aussi absolument décrypter tous les mécanismes cellulaires afin de comprendre pourquoi cette thérapie est régénératrice. Chaque nouvelle étude scientifique à ce sujet est un pas de plus vers l’utilisation et la démocratisation de cette thérapie pour soigner le cerveau.
Le caisson hyperbare, pour qui et pourquoi ?
N’hésitez pas à consulter ces quelques articles au sujet de l’utilisation de l’oxygénothérapie hyperbare sur différentes pathologies :
- L’oxygénothérapie hyperbare, un traitement pour la paralysie cérébrale
- L’oxygénothérapie hyperbare pour améliorer les symptômes liés à l’autisme
- Exemple d’un traumatisme crânien soigné avec l’oxygénothérapie hyperbare
- Soigner un cerveau à l’aide d’un caisson hyperbare
- AVC et oxygénothérapie hyperbare : les résultats sur 3 patients
- Fibromyalgie et oxygénothérapie hyperbare : douleurs réduites
- Une victime de noyade soignée avec 40 séances de caisson hyperbare
- Les incroyables progrès cognitifs d’Annie grâce au caisson hyperbare
Comment mettre en place l’oxygénothérapie hyperbare à la maison ?
Si vous souhaitez mettre en place cette thérapie chez vous, je peux vous conseiller et vous accompagner. Les protocoles que je propose se basent sur les dernières avancées scientifiques ainsi que sur mon expérience sur le sujet.
J’anime aussi un groupe Facebook sur le sujet, dans lequel vous pouvez poser vos questions :
Voici un article similaire qui devrait vous intéresser
Sources scientifiques utilisées pour la rédaction de cet article
- 1https://www.ncbi.nlm.nih.gov/pmc/articles/PMC34224/
- 2https://pubmed.ncbi.nlm.nih.gov/18036551/
- 3https://www.nobelprize.org/prizes/medicine/1938/heymans/facts/
- 4https://www.nobelprize.org/prizes/medicine/2019/summary/
- 5https://fr.wikipedia.org/wiki/Facteur_de_transcription
- 6https://en.wikipedia.org/wiki/Hypoxia-inducible_factor
- 7https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6586788/
- 8https://pubmed.ncbi.nlm.nih.gov/18504100/
- 9https://pubmed.ncbi.nlm.nih.gov/19698058/
- 10https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6453877/
- 11https://www.frontiersin.org/articles/10.3389/fphys.2021.752117/full
- 12https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7355982
- 13https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4102647
- 14https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5021505/
- 15https://pubmed.ncbi.nlm.nih.gov/18644387/
- 16https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5654341/
- 17https://pubmed.ncbi.nlm.nih.gov/28779582/
- 18https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5489129/
- 19https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4084443
- 20https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4968589
- 21https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6630002